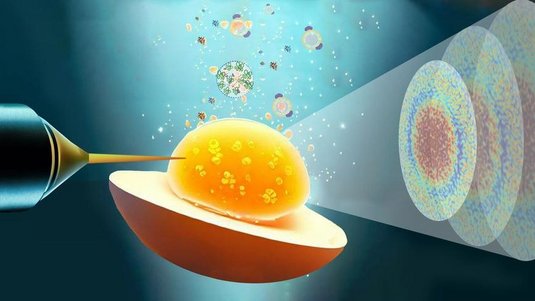
„Dreidimensionales Modell der Herzmuskelzelle“
Manuel Kreye
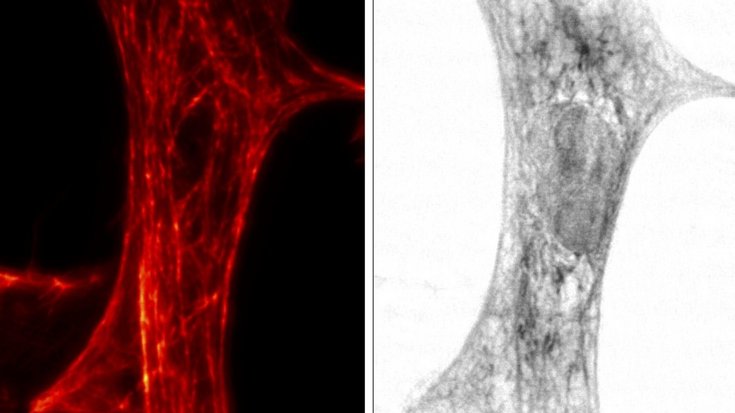
Marten Bernhardt et al./Universität Göttingen
Vom Herzmuskel erwarten wir lebenslang eine einwandfreie mechanische Funktion. Wie die Kontraktion auf zellulärer und molekularer Ebene genau abläuft, welche strukturellen Änderungen mit Krankheiten verbunden sind und wie sich Herzgewebe auch künstlich erzeugen lässt, ist Gegenstand intensiver interdisziplinärer Forschung. Um die Strukturen innerhalb von Herzmuskelzellen mit hoher Auflösung und unterschiedlichen Kontrasten abzubilden, kombinieren Tim Salditt und seine Kollegen von der Universität Göttingen verschiedene Mikroskopiemethoden. In einem vom Bundesforschungsministerium geförderten Projekt bauen sie dazu eine neue Experimentierstation an der Röntgenlichtquelle PETRA III am Forschungszentrum DESY in Hamburg auf. Darüber sprach Welt der Physik mit Tim Salditt.
Welt der Physik: Wie gehen Sie vor, um Herzmuskelzellen zu untersuchen?
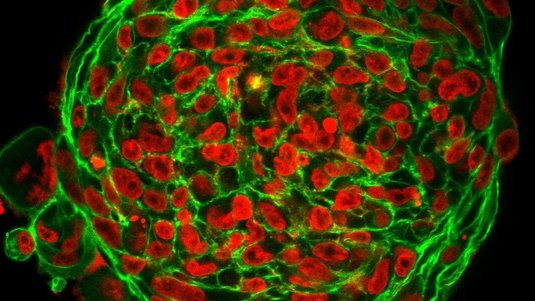
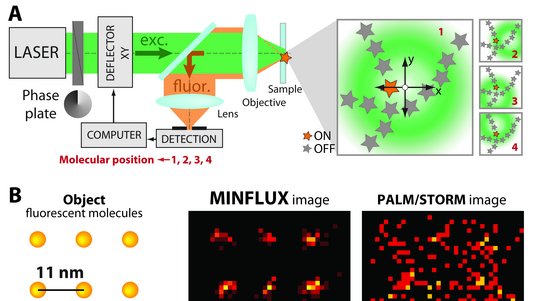
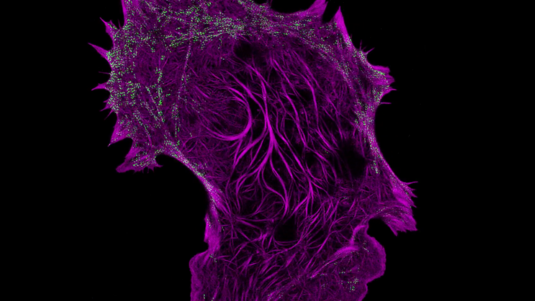
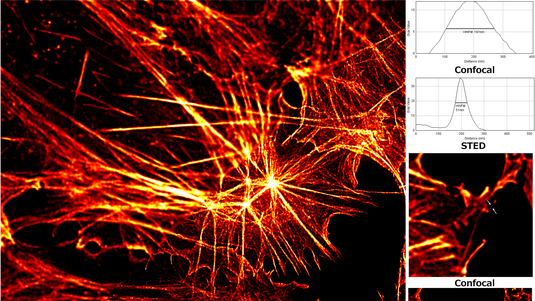
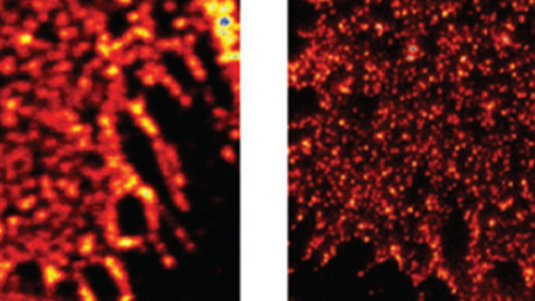
Tim Salditt: Zunächst untersuchen wir die Zellstrukturen mit hochauflösenden Lichtmikroskopen. Hier eignet sich besonders das sogenannte STED-Mikroskop – für dessen Entwicklung Stefan Hell im Jahr 2014 den Nobelpreis für Chemie erhielt. Wir markieren ein bestimmtes Molekül innerhalb der Zelle mit einem Farbstoff und mithilfe des STED-Mikroskops erkennen wir, wo sich dieses Molekül innerhalb der Zelle befindet. Es gibt aber auch Strukturmerkmale von Zellen, die sich nicht anfärben lassen oder so klein sind, dass wir sie mit dieser Methode nicht untersuchen können.
Gibt es dafür andere Methoden?
Ja, mithilfe der sogenannten Röntgenbeugung lassen sich auch molekulare Strukturmerkmale von Zellbestandteilen aufklären. Dafür nutzen wir die Welleneigenschaften der Röntgenstrahlung. Denn trifft Röntgenstrahlung auf ein Molekül innerhalb einer Zelle, wird die Welle an den Elektronen des Moleküls gebeugt und es entstehen neue kleinere Wellen. Dieses Phänomen lässt sich beispielsweise auch bei Wasserwellen auf einer Teichoberfläche beobachten. Treffen kreisförmige Wasserwellen etwa auf einen Stein, entstehen neue Wellen, die sich überlagern und so ein charakteristisches Muster bilden.
Wie lässt sich das experimentell umsetzen?
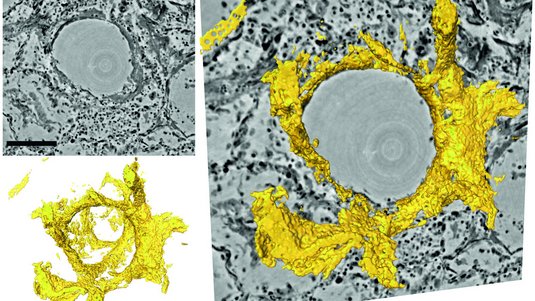
In unserem aktuellen Verbundprojekt nutzen wir die Röntgenstrahlungsquelle PETRA III in Hamburg. Dort wird in einem Ringbeschleuniger sehr energiereiche Röntgenstrahlung erzeugt, die sich so weit fokussieren lässt, dass nur einzelne Zellbestandteile belichtet werden. Mit einem Detektor nehmen wir dann die Muster auf, die durch die Röntgenbeugung entstehen, und können damit auf die Struktur rückschließen. Molekulare Strukturen können wir also nicht direkt abbilden, sondern nur indirekt erschließen. Größere Objekte, etwa Bündel aus Proteinfasern oder Bestandteile im Zellkern, lassen sich dagegen auch direkt abbilden – mit einer Methode, die man als Röntgenholografie bezeichnet.
Wie rekonstruieren Sie aus den Beugungsmustern die molekulare Struktur der untersuchten Probe?
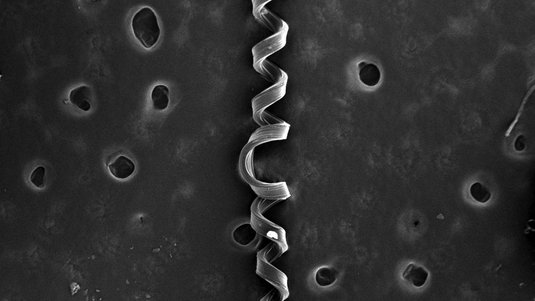
Das ist eine interessante mathematische Aufgabe. Wir haben sehr viel Zeit in die Entwicklung von Algorithmen gesteckt, mit denen sich mittlerweile sehr genaue Abbilder – beispielsweise von biologischen Zellen – am Computer berechnen lassen. Diese Messdaten kombinieren wir dann mit den Ergebnissen der STED-Mikroskopie. Wenn wir zudem die gesamte Zelle aus einer ganzen Reihe von Winkeln und Positionen vermessen, können wir am Ende die vereinten Daten der STED-Mikroskopie und der Röntgenholografie zu einem dreidimensionalen Modell der Herzmuskelzelle zusammensetzen.
Wie ist der aktuelle Stand des Projekts und was sind die nächsten Schritte?
Gerade haben wir über die optischen Messmethoden und die Datenauswertung in der Zeitschrift „Nature Communications“ berichtet. Und jetzt beginnen wir, an lebenden Zellen zu arbeiten. Das bringt natürlich ein paar Schwierigkeiten mit sich, denn die Zellen bewegen sich unter Umständen im Strahl und müssen deshalb sehr viel kürzer belichtet werden. Eine weitere Schwierigkeit ist, dass wir lebende Zellen nur einer bestimmten Dosis an Röntgenstrahlung aussetzen können. Wenn wir diese Dosis übersteigen, werden Zellteile zerstört oder die Zellen können sterben. Diese Aspekte des Strahlenschadens versuchen wir gerade aufzuklären. Aber insgesamt funktioniert unsere Methode schon so gut, dass sich bereits andere Arbeitsgruppen dafür interessieren und Messzeiten beantragen.
Was ließe sich denn mit der von Ihnen entwickelten Methode noch erforschen?
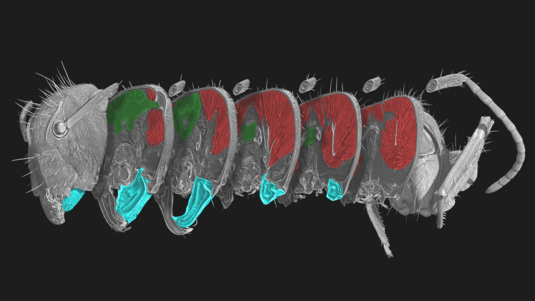
Es kommen beispielsweise Biologen, die sich fragen, was in einem Insektenauge passiert, wenn Licht hineinfällt. Diese Forscher haben bisher ganz andere Messtechniken eingesetzt, bei denen die Probe meist in dünne Scheiben zerlegt werden muss. Hier bietet unsere Methode einen Vorteil, da die dreidimensionale Struktur der Proben erhalten bleibt. In ein paar Wochen kommt auch eine neurowissenschaftliche Gruppe, die sich für die Struktur von Nervenzellen zwischen der linken und der rechten Hirnhälfte interessiert. Es ist schön, als Physiker auch einmal in einem Feld mit ganz anderen Fragestellungen zu arbeiten.
Das Bundesministerium für Bildung und Forschung fördert das Projekt „Strukturanalyse in biologischen Zellen: Rasterkleinwinkelstreuung und Diffraktion mit nano-fokussierter Undulatorstrahlung“ im Zeitraum von Juli 2016 bis Juni 2019 mit rund einer halben Million Euro.
Fördersumme: 520 790 Euro
Förderzeitraum: 01.07.2016 bis 30.06.2019
Förderkennzeichen: 05K16MG2
Beteiligte Institutionen: Universität Göttingen
Quelle: https://www.weltderphysik.de/thema/bmbf/erforschung-kondensierter-materie/dreidimensionales-modell-der-herzmuskelzelle/