Quantenmechanik und Unschärferelation
Maike Pollmann
Atome, Elektronen und anderen Quantenteilchen verhalten sich grundlegend anders als wir es aus unserem Alltag kennen. Sie besitzen sowohl Teilchen- als auch Welleneigenschaften, ihre Zukunft ist absolut unbestimmt und selbst wenn man im Jetzt misst, ist das Ergebnis nicht in jedem Fall präzise.
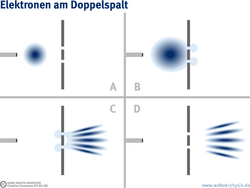
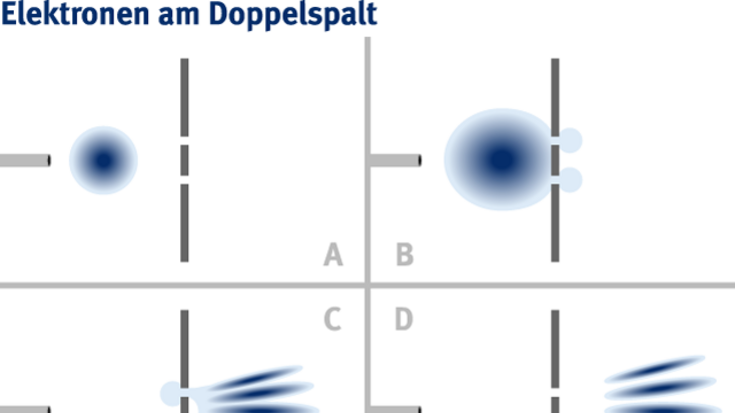
Die uns bekannte Materie besteht aus Atomen, Elektronen und anderen Quantenteilchen. Und doch könnten die in der mikroskopischen Teilchenwelt und der makroskopischen Welt der Körper geltenden Gesetze verschiedenartiger nicht sein. Besonders eindrucksvoll zeigen sich die Eigenarten der Quantenteilchen im Doppelspaltversuch: Ein Elektronenstrahl trifft auf eine Blende mit zwei schmalen, parallelen Spalten, dringt durch diese hindurch und landet auf einer dahinter montierten Fotoplatte. Jedes auftreffende Teilchen schwärzt diese Platte an der Auftreffstelle und hinterlässt dort einen gut lokalisierbaren schwarzen Punkt.
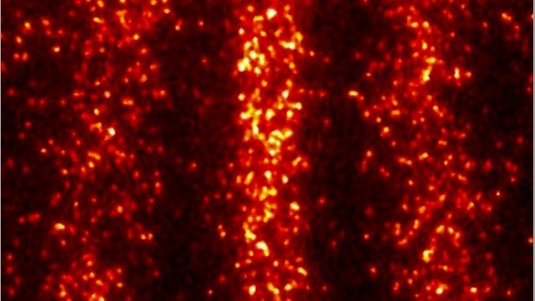
Insoweit verhalten sich Elektronen nicht anders als makroskopische Partikel wie etwa Sandkörner und demonstrieren so ihre Teilcheneigenschaften. Nach hinreichend vielen Treffern zeigt sich allerdings ein wesentlicher Unterschied: Während Sandkörner zwei separate Haufen hinter dem Doppelspalt bilden, da sie entweder durch den linken oder aber den rechten Spalt geflogen sind, erzeugen die Elektronen auf der Fotoplatte ein strukturiertes Schwärzungsmuster, das aus Streifen unterschiedlicher Intensität besteht (siehe Abbildung rechts).
Dieses sogenannte Interferenzmuster kennt man auch von Licht- oder Wasserwellen, wenn man sie durch einen ähnlichen Doppelspalt laufen lässt. Und tatsächlich lässt sich auch das Entstehen des Elektronen-Auftreffmusters mithilfe einer Wellentheorie beschreiben. Im Gegensatz zu Sandkörnern besitzen Elektronen also auch Welleneigenschaften. Übrigens gilt dies gleichermaßen für andere Quantenteilchen wie Protonen, Neutronen, Atome und sogar für Fullerene – komplexe Moleküle aus 60 Kohlenstoffatomen. Sie alle erzeugen im Doppelspaltversuch das charakteristische Interferenzmuster. Die klassisch-physikalische Betrachtungsweise scheitert daran, diesen „Teilchen-Welle-Dualismus“ zu erklären.
Erst die Quantenmechanik von Werner Heisenberg, Erwin Schrödinger und anderen lieferte Konzepte zum Verständnis: Quantenteilchen muss man durch eine Wellenfunktion beschreiben! 1929 schlug der deutsche Physiker Max Born eine Wahrscheinlichkeitsinterpretation der quantenmechanischen Wellenfunktion vor. Genauer gesagt entspricht das Quadrat dieser Wellenfunktion der Wahrscheinlichkeit, mit der sich ein Teilchen gerade an diesem oder jenem Ort aufhält, dort also gemessen werden würde.
Echter Zufall
Für den Doppelspaltversuch heißt das: Bevor ein Elektron auf die Fotoplatte trifft und somit durch die lokale Schwärzung seine Position als gemessen anzusehen ist, lassen sich für den Aufenthaltsort dieses Teilchens nur bestimmte Wahrscheinlichkeiten angeben – und diese lassen sich mithilfe der Elektronen-Wellenfunktion berechnen. Diese ist übrigens im Allgemeinen räumlich stark ausgedehnt; prinzipiell könnten sich die Elektronen eines bei DESY stehenden Doppelspaltexperiments sogar in Amerika befinden – die Wahrscheinlichkeit dafür ist allerdings verschwindend gering. Sehr viel wahrscheinlicher ist es dagegen, dass sich die Elektronen durch einen der beiden Spalte bewegen, sofern sich ihre Wellenfunktion in diese Richtung ausbreitet. Geschieht das senkrecht zur Blende und symmetrisch zu den beiden Spalten darin, liegt die Aufenthaltswahrscheinlichkeit in jedem Spalt bei 50 Prozent. Hinter der Blende überlagern sich die Teilwellen aus den beiden Spalten – genauso wie bei einer Wasser- oder Lichtwelle – und bilden dort durch gegenseitige Verstärkung der Wellenberge und Auslöschung in den Wellentälern ein Interferenzmuster.
Für die Aufenthaltswahrscheinlichkeit, die sich ja aus dem Quadrat der Wellenfunktion ergibt, bedeutet das: An Stellen, wo sich die Teilwellen verstärken, treffen die Elektronen wahrscheinlicher auf als an solchen, wo sich die Teilwellen nahezu auslöschen. Wo genau auf der Fotoplatte sich ein Elektron dann tatsächlich „materialisiert“ – also ein realer schwarzer Fleck auf der Fotoplatte entsteht –, entscheidet sich erst im Moment des Auftreffens und ist nicht vorhersagbar.
Hierin liegt ein wesentlicher Unterschied zwischen makroskopischen und mikroskopischen Objekten. In unserer makroskopischen Alltagswelt lässt sich alles im Voraus berechnen – sogar die Lottozahlen am kommenden Samstag. Man müsste dafür nur alle entscheidenden Größen wie etwa die Position der Kugeln, die Geschwindigkeit der Trommel und so weiter im Vorfeld kennen. Der vermeintliche Zufall beruht hier also nur auf einem Mangel an Informationen über die Anfangswerte, allerdings auch an unserem Unvermögen, die komplexe Dynamik so vieler Größen dann auch auszuwerten.
Im Fall der Elektronen im Doppelspaltversuch (und generell aller Quantenteilchen) würde aber selbst eine genaue Kenntnis der Wellenfunktion nichts nützen: Vollkommen identisch präparierte Teilchen treffen an verschiedenen Stellen der Fotoplatte auf – die Wellenfunktion liefert nur die Wahrscheinlichkeiten dafür. Allein der (echte) Zufall entscheidet, wo die Teilchen tatsächlich landen. Läuft allerdings eine Vielzahl solcher Quanten durch den Doppelspalt, wird die Trefferverteilung auf der Platte reproduzierbar: Bei jedem Durchlauf entsteht das charakteristische Schwärzungsmuster aus dunklen und hellen Streifen, das sich mithilfe der Wellentheorie beschreiben lässt.
In Überlagerung
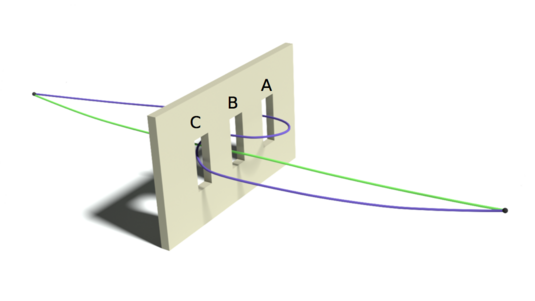
Das Doppelspaltexperiment lässt schon erahnen, dass man den klassischen Bahnbegriff in der Quantenwelt aufgeben muss. Während Sandkörner durch einen der beiden Spalte laufen, scheinen Quantenteilchen gleichzeitig durch beide zu dringen – ihre Wellenfunktion macht nämlich genau das: Die Interferenzeffekte der Wellenfunktion nach der Blende lassen sich auch dann beobachten, wenn die Elektronen einzeln nacheinander durch die Anordnung geschickt werden. Was aber passiert, wenn man direkt hinter den Spalten experimentell „nachschaut“, welchen Weg ein Teilchen tatsächlich gewählt hat?
Beobachtete man viele Teilchendurchläufe, würde man eine Hälfte hinter Spalt 1 und die andere hinter Spalt 2 finden. Das deckt sich mit der berechneten Aufenthaltswahrscheinlichkeit, die in jedem Spalt bei 50 Prozent liegt (die oben genannte Symmetrie des Experiments vorausgesetzt). Das Schwärzungsmuster auf der Fotoplatte wäre nun allerdings ein anderes: Statt des typischen Streifenmusters entstehen auf dem Schirm zwei „Elektronenhaufen“ - ähnlich zum klassischen Fall.
Verantwortlich für das veränderte Muster ist die Messung, durch welchen Spalt die jeweiligen Elektronen gelaufen sind. Sie verändert nämlich die Wahrscheinlichkeits-Wellenfunktion der Elektronen. Denn die Teilchen werden auf einen der beiden möglichen Spaltdurchgänge festgelegt. Für die Wellenfunktion bedeutet das: Statt eines Überlagerungszustands aus Teilwellen durch die beiden Spalte existieren nunmehr hinter der Blende die beiden Zustände mit jeweils bekanntem Weg, die nicht mehr interferieren können. Folglich verschwindet auch das Interferenzmuster, das ja aus der Überlagerung der beiden Teilwellen resultierte. Bei symmetrischer Messanordnung treffen die Teilchen mit einer Wahrscheinlichkeit von 50 Prozent hinter Spalt 1 beziehungsweise Spalt 2 auf.
Die Messung der Wegalternativen beeinflusst also – anders als in unserer Alltagswelt – die Wellenfunktion und damit die Aufenthaltswahrscheinlichkeiten der Quantenteilchen. Das gilt nicht nur für den Ort der Teilchen, sondern zum Beispiel auch für ihre Impulse oder Drehimpulse. Solange die Wellenfunktion der Quantenteilchen nicht durch eine Messung „gestört“ wird, enthält sie alle möglichen Messergebnisse in einer Überlagerung. Eine Messung lässt die Menge an möglichen Werten zusammenschrumpfen.
Unbestimmtheitsrelation
Eine weitere Eigenheit der Quantenwelt tritt auf, wenn man bestimmte Eigenschaften eines Teilchens gleichzeitig misst. Gewisse physikalische Größen – das prominenteste Paar sind Ort und Impuls – lassen sich nicht gleichzeitig exakt angeben, egal wie genau man auch zu messen trachtet. Das heißt etwa: Ist die Position eines Teilchens sehr genau bekannt, ist seine Geschwindigkeit weitgehend unbestimmt. Umgekehrt wissen wir kaum etwas von seinem Aufenthaltsort, wenn wir seine Geschwindigkeit sehr genau kennen.
Der Physiker Werner Heisenberg beschrieb diese für Quantenteilchen charakteristische Gesetzmäßigkeit im Jahr 1927 mit seiner berühmten Unschärferelation:
$$\Delta x \cdot \Delta p \geq \frac{h}{4\pi}$$
wobei \(\Delta x\) die Ortsunschärfe, \(\Delta p\) die Impulsunschärfe und \( h \)das Plancksche Wirkungsquantum – eine für die Quantenphysik unentbehrliche, sie geradezu kennzeichnende Naturkonstante – sind. Durch diesen Zusammenhang von Orts- und Impuls-Messunschärfe lässt sich eingrenzen, wie ungenau die beiden Messergebnisse mindestens sein werden, ja zwangsläufig sein müssen, wenn beide Größen gleichzeitig gemessen werden.
Die Orts-Impuls-Unschärferelation gilt als eines der Grundprinzipien der Quantenmechanik. Neben diesen beiden physikalischen Größen finden sich in der Quantenwelt auch noch andere Paare, die eine solche Unschärferelation erfüllen – etwa verschiedene Drehimpulskomponenten. Wichtig ist, dass diese Art von Unschärfe nicht allein aus Messungenauigkeiten oder Messfehlern resultiert. Sie ist eine unausweichliche Konsequenz der mathematischen Struktur der Quantenphysik, aus der sie sich unabhängig von konkreten Experimenten ableiten lässt.
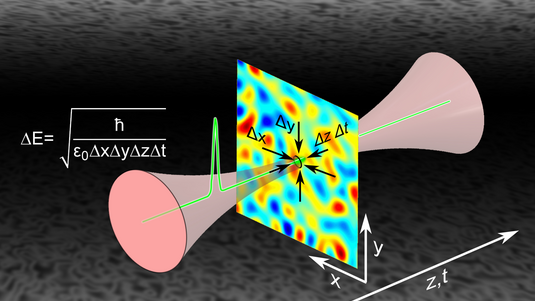
Einen tiefer greifenden Artikel über Heisenbergs Unschärferelation sowie zur Energie-Zeit-Unschärfe finden Sie hier.
Bohrsches Atommodell überholt
Das am Beginn des vorigen Jahrhunderts formulierte Bohrsche Atommodell besagt, dass die Atome aus einem Atomkern und Elektronen bestehen, die den Kern auf bestimmten Kreis- oder Ellipsenbahnen umrunden. Diese Vorstellung hält sich noch heute hartnäckig in den Köpfen vieler Leute. Doch so anschaulich es auch sein mag – es ist leider falsch. Es geht nämlich davon aus, dass sich die Elektronen auf definierten Bahnen bewegen und damit jederzeit einen gleichzeitig genau festgelegten Ort und Impuls besitzen.
Damit aber widerspricht das Bohrsche Modell der Heisenbergschen Unschärferelation, wonach diese beiden Größen in der Quantenwelt nie gleichzeitig scharf angegeben werden können. Anstelle von Bahnen lassen sich nur gewisse Aufenthaltswahrscheinlichkeiten für die Elektronen in der Umgebung des Atomkerns angeben. Diese folgen aus der Wellenfunktion, die den quantenmechanischen Zustand der Elektronen in einem Atom beschreibt.
Untersucht man in einem Atom die Orte gleicher Elektronenaufenthaltswahrscheinlichkeit, so ergeben sich kunstvolle Gebilde aus Keulen und Kugeln, sogenannte Orbitale. Für gewöhnlich werden die Raumbereiche angegeben, in denen sich das Elektron mit einer Wahrscheinlichkeit von 90 Prozent aufhält. Je nachdem, in welchem Energiezustand sich das Teilchen befindet, besiedelt es ein anderes Orbital.
Durch diese „moderne“ Vorstellung eines Atoms, bestehend aus dem Atomkern und einer „Wahrscheinlichkeitswolke“ für die Elektronen darum herum, können Wissenschaftler beispielsweise erklären, wie verschiedene Atome chemisch miteinander reagieren und warum sich Moleküle in einer bestimmten Weise zusammensetzen – wieso sich zum Beispiel Graphen, wofür es jüngst den Nobelpreis gab, bildet und warum Eiweißmoleküle zusammenhalten, die die Grundlage unseres Lebens bilden und vieles, vieles mehr.
Welt der Physik
Quelle: https://www.weltderphysik.de/gebiet/teilchen/quanteneffekte/grundlagen/