„Man braucht viel Geduld“
Dirk Eidemüller

Intermedial Design für GSI/FAIR
Anfang des 19. Jahrhunderts entwickelte sich ein zunehmendes Interesse an den bis dahin bekannten chemischen Elementen. Forscher entdeckten, dass die Eigenschaften eines Elements mit der Größe und dem Gewicht der jeweiligen Atome zusammenhängen. 1869 veröffentlichten Dmitri Iwanowitsch Mendelejew in Sankt Petersburg und Julius Lothar Meyer in Karlsruhe unabhängig voneinander die ersten Periodensysteme. Mittlerweile wurden viele weitere Elemente in das Periodensystem aufgenommen – unter anderem auch solche, die sich nur künstlich im Labor erzeugen lassen. Welt der Physik sprach darüber mit Sigurd Hofmann vom GSI Helmholtzzentrum für Schwerionenforschung in Darmstadt, der an der Entdeckung einiger neuer Elemente beteiligt war.
Welt der Physik: Was ist ein chemisches Element?
Sigurd Hofmann: Alle Atome eines chemischen Elements besitzen die gleiche Anzahl von negativ geladenen Elektronen, die sich um den Atomkern bewegen. Da ein Atom elektrisch neutral ist, entspricht die Anzahl der Elektronen der Anzahl der positiv geladenen Protonen im Atomkern. Die Elektronen sind um den Atomkern in sogenannten Elektronenschalen angeordnet, die sich nacheinander füllen. Ist eine Schale mit Elektronen voll besetzt, dann ist die Bindung stark und das Atom reagiert nur sehr träge mit anderen Atomen. Dies trifft auf alle Edelgase zu. Untereinander ähnliche chemische Eigenschaften besitzen auch alle Atome mit der gleichen Anzahl von Elektronen außerhalb einer abgeschlossenen Schale.
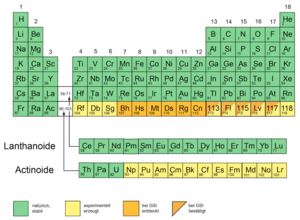
Wie sind die Elemente im Periodensystem angeordnet?
Das Periodensystem greift die Anordnung der Elektronen um den Atomkern auf. In der ersten Spalte stehen die Elemente mit einem Elektron außerhalb einer voll besetzten Schale, in der zweiten die mit zwei Elektronen und so fort. Ganz rechts, in der 18. Spalte, stehen die Edelgase. Am GSI Helmholtzzentrum für Schwerionenforschung wurden die Elemente mit den Ordnungszahlen von 107 bis 112 erstmals erzeugt und nachgewiesen. Im Periodensystem stehen diese Elemente in den Spalten 7 bis 12 und gehören zu den superschweren Kernen. Im Zentrum des Interesses standen zunächst nicht die chemischen Eigenschaften dieser Elemente, sondern ob und auf welche Art und Weise die entsprechenden Atomkerne gebildet werden können.
Wie lassen sich denn neue Atomkerne erzeugen?
Superschwere Atomkerne lassen sich am besten erzeugen, indem man einen Strahl aus mittelschweren und elektrisch geladenen Atomen auf ein schweres Element schießt. Wenn dieser Ionenstrahl energiereich genug ist, können die stark positiv geladenen Atomkerne ihre elektrische Abstoßung überwinden und sich zu einem einzigen Atomkern vereinigen. Gerade bei den schwersten Elementen hat man aber mit dem Problem zu kämpfen, dass überhaupt nur wenige Atome entstehen, die dann meist auch noch sehr schnell zerfallen.
Wie hoch ist die Produktionsrate für neue Atome?
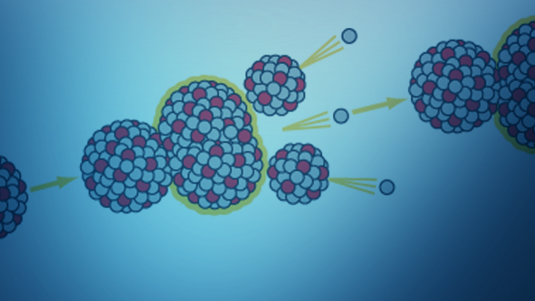
Das hängt von vielen Faktoren ab, unter anderem von den gewählten Atomkernen und davon, ob die Strahlenergie genau richtig eingestellt ist. Ist sie zu niedrig, treffen die Kerne nie aufeinander. Ist sie zu hoch, zerplatzen beide Kerne, anstatt sich zu vereinigen. Aber selbst wenn sie in Verbindung treten, ist noch lange nicht gesagt, dass ein neuer Atomkern mit dem gesamten Material aus den beiden Ausgangskernen entsteht. Dies passiert nur etwa in einem von einer Million Fällen. Die große Mehrheit dieser Ereignisse führt lediglich dazu, dass einige Protonen und Neutronen von einem Kern auf den anderen übergehen.
Ab wann spricht man überhaupt von dem Nachweis eines neuen Elements?
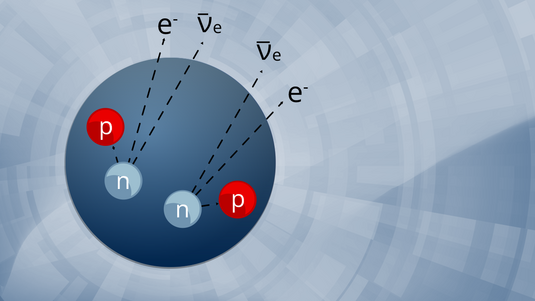
Wenn sich die beiden Atomkerne vereinigt haben, reicht das noch nicht aus, um von einem neuen Element zu reden. Für den Nachweis eines Elements muss der Atomkern im energetischen Grundzustand vorliegen. Direkt nach der Vereinigung befindet er sich aufgrund der eingebrachten Energie aber in einem angeregten und damit instabilen Zustand. In den allermeisten Fällen spaltet sich ein solcher Atomkern nach sehr kurzer Zeit und platzt. In wieder nur rund einem von einer Million Fällen „schwitzt“ der Kern aber Neutronen aus und gibt die überschüssige Energie durch Gammastrahlung wieder ab – bis er sich im Grundzustand befindet.
Wie lange dauerte es ungefähr, die neuen Elemente zu identifizieren?
Die Produktionsraten liegen mitunter bei nur wenigen Atomkernen pro Monat. Man braucht also viel Geduld. Von Element 113, Nihonium, tauchten nach einer Messzeit von zwei Jahren gerade einmal drei Atome auf. Bei den jüngsten Elementen – von Flerovium mit der Ordnungszahl 114 bis Oganesson, Element 118 – sehen wir aber Anzeichen, dass wir uns der sogenannten Insel der Stabilität genähert haben. In diesem Bereich des Periodensystems – bei den schwersten erzeugbaren Elementen – sind die Atomkerne zwar immer noch instabil, aber etwas langlebiger als ihre leichteren Nachbarn.
Die Entdeckung des letzten neuen Elements ist schon ein paar Jahre her. Steht bald wieder eine Überraschung an?
Wann genau das nächste schwere Element identifiziert wird, lässt sich schwer sagen. Je schwerer die Elemente werden, desto diffiziler wird es, sie überhaupt erst zu erzeugen und dann auch noch nachzuweisen. Es gab in der Vergangenheit aber immer wieder einmal Streit, welche Kollaboration als Erste dieses oder jenes Element nachgewiesen hat. Deshalb haben wir uns in einer internationalen Arbeitsgruppe zusammengesetzt, um den experimentierenden Kollegen klare Kriterien an die Hand zu geben, an denen sie sich nun orientieren können.
Quelle: https://www.weltderphysik.de/gebiet/teilchen/hadronen-und-kernphysik/man-braucht-viel-geduld/