So fest kleben Moleküle auf der Oberfläche
Lisa Leander
Jülich – Haftet ein Molekül an einer Oberfläche, überlagern sich dabei die Kräfte von Bindungen und Wechselwirkungen zwischen den Atomhüllen. Deshalb konnten Wissenschaftler bisher nur grob ermitteln, wie stark verschiedene organische Moleküle an der Fläche gehalten werden. Mit der feinen Spitze eines Rasterkraftmikroskops erhielt eine Forschergruppe jetzt genauere Messwerte, die anschließend durch Computersimulationen bestätigt wurden. Dabei stellten die Wissenschaftler fest, dass sich die einzelnen Bindungstypen unterschiedlich stark abschwächen, wenn das Molekül von der Fläche abgezogen wird.
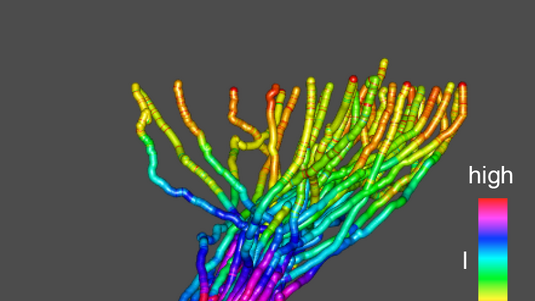
Das Team von Forschungszentrum Jülich verwendete als Molekül Perylentetracarbonsäuredianhydrid (PTCDA), das aus sieben Kohlenstoffringen besteht, an deren Enden Sauerstoffatome gebunden sind. Das PTCDA-Molekül lag auf einer Goldunterlage, an einem Ende war es mit einem Rasterkraftmikroskop verbunden. Die Spitze des Mikroskops bestand nur aus einem einzelnen Atom und war zusätzlich an einer Quarzstimmgabel befestigt. Zieht man das Molekül schrittweise von der Oberfläche ab, verändern die wirkenden Kräfte die Frequenz, mit der die Mikroskopspitze schwingt.
„Den Messungen zufolge beträgt die Bindungsenergie eines solchen Einzelmoleküls an eine Goldoberfläche rund 2,5 Elektronenvolt (eV) und nicht 2,0 eV, wie durch frühere Berechnungen vorhergesagt,“ berichtet Christian Wagner vom Forschungszentrum Jülich. „Diese Energie reicht gerade aus, um ein Staubkorn um den Durchmesser eines Wasserstoffatoms anzuheben.“ Ein Großteil der Energie, etwa 100 Millielektronenvolt, gehe auf Van-der-Waals-Kräfte zurück. Im Gegensatz zu einer chemischen Bindung müssen sich die Elektronenwolken von Molekül und Oberfläche bei der Van-der-Waals-Kraft nicht überlappen. Die Wechselwirkung entsteht vielmehr dadurch, dass die Elektronen in den Wolken nicht gleichmäßig verteilt sind. Diese Ladungsverteilungen beeinflussen sich gegenseitig und verschieben die Elektronen so noch stärker.
Die Messungen ergaben, dass die Van-der-Waals-Kräfte bei der Verbindung von Molekül und Oberfläche am längsten nachwirken. „Entfernt man ein Molekül kontinuierlich von der Oberfläche, so spürt es anfänglich noch alle Wechselwirkungen, aber schon nach einigen Nanometern bleibt nur die Van-der-Waals-Anziehung übrig,“ erklärt Wagner. Um ihre Ergebnisse zu bestätigen, berechneten die Wissenschaftler mit dem Jülicher Großrechner JUDGE insgesamt 100 Millionen Bindungspotenziale, bei 4000 davon konnten sie das Ablösen des Moleküls komplett simulieren.
Wagner und seine Kollegen sehen in ihrem neuen Messverfahren einen Fortschritt für die Oberflächenphysik. Es könne daher in vielen Gebieten wie etwa der Pharma- oder Energiephysik von Nutzen sein.
Quelle: https://www.weltderphysik.de/gebiet/teilchen/nachrichten/2012/so-fest-kleben-molekuele-auf-der-oberflaeche/