Bewegung von einzelnen Zellen verfolgt
Universität Göttingen
Wissenschaftler der Universität Göttingen haben ein neues Verfahren entwickelt, mit dem sich Zellen mit einer bislang unerreichten Auflösung beobachten lassen. Das optisch-spektroskopische Verfahren nutzt einen physikalischen Effekt, bei dem Energie von einem angeregten Farbstoffmolekül auf einen Metallfilm übertragen wird. Dadurch wird es möglich, die Bewegung einzelner Zellen mit einer räumlichen Auflösung im Bereich von Nanometern in Echtzeit zu verfolgen. Bisher konnten Formänderungen lebender Zellen typischerweise nur mit einer 1000-mal schlechteren Genauigkeit beobachtet werden. Die Studie wurde in der Fachzeitschrift „Nature Photonics“ veröffentlicht.
Zellen sind die Grundbausteine aller lebenden Organismen, und Erkenntnisse über ihre Struktur, Funktion und Wechselwirkung sind ein zentrales Anliegen der modernen biologischen Forschung. Die Wissenschaftler gehen dabei unter anderem der Frage nach, wie sich Zellen fortbewegen und dadurch miteinander in Kontakt kommen und Zellverbünde bilden können. „Bei der Untersuchung dieser Prozesse möchten wir die Formänderung und Bewegung der Zellen mit möglichst hoher räumlicher Auflösung verfolgen können“, erläutert Jörg Enderlein von der Universität Göttingen. Dazu müssen die Forscher in der Lage sein, Abstände auf der Ebene von Molekülen genau zu messen.
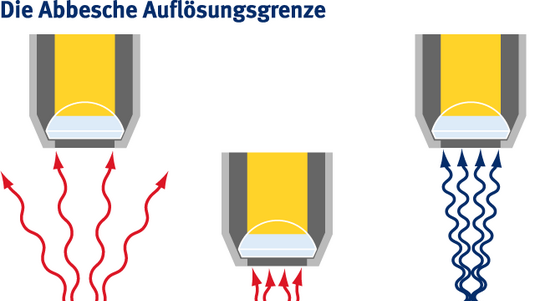
Die von Enderlein und seinen Kollegen entwickelte Methode nutzt einen physikalischen Effekt, der bereits in den 1970er- und 1980er-Jahren eingehend untersucht wurde: Bringt man ein fluoreszierendes Farbstoffmolekül in die Nähe eines Metalls, so überträgt sich seine Anregungsenergie auf das Metall. Dieser Energieaustausch bewirkt, dass das Leuchten im Molekül schneller erlischt. Aus der Fluoreszenzdauer lässt sich auf den Abstand zwischen Molekül und Metallschicht schließen, da die Geschwindigkeit der Energieübertragung von diesem Abstand abhängt.
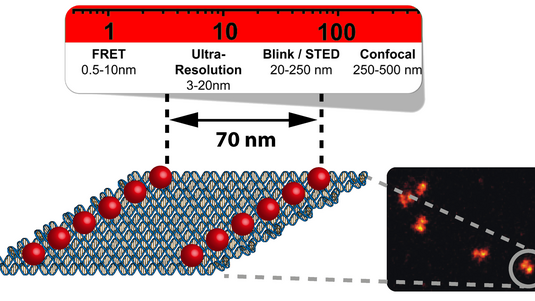
Als bisher beste Messmethode gilt der sogenannte Förster-Resonanzenergietransfer, der anstelle einer Metallschicht ein zweites Farbstoffmolekül für die Energieübertragung verwendet. Allerdings dürfen die beiden Farbstoffmoleküle nicht weiter als zehn Nanometer voneinander entfernt sein, denn nur in diesem Bereich kann überhaupt Energie übertragen werden. Zudem hängen die Messergebnisse davon ab, wie die Moleküle räumlich zueinander orientiert sind. Beim vorgestellten neuen Verfahren – dem sogenannten metallinduzierten Energietransfer – genügt es, eine Metallschicht bis auf etwa hundert Nanometer an das Molekül heranzubringen. Für die Aufnahmen von lebenden Zellen mit einer Fluoreszenz-Markierung reichen dann ein gewöhnliches Konfokalmikroskop und ein metallbeschichtetes Deckgläschen.
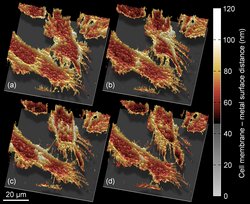
Indem sie den Abstand zwischen den Zellen und der Metallschicht maßen, gelang es den Forschern, die Membranen lebender Zellen nanometergenau abzubilden. Durch eine zeitaufgelöste Bildgebung konnten sie zudem die Bewegungen der Zellen in Echtzeit verfolgen. „Unser Verfahren eröffnet nicht nur völlig neue Möglichkeiten für die Untersuchung von Zellbewegungen, sondern es dürfte auch in vielen anderen Forschungsgebieten, wo höchste räumliche Auflösung dynamischer Prozesse erwünscht ist, breite Anwendung finden“, so Enderlein.
Pressemitteilung
Quelle: https://www.weltderphysik.de/gebiet/leben/nachrichten/2014/bewegung-von-einzelnen-zellen-verfolgt/