Lichtblicke in die Nanowelt
Björn Gojdka
Das Lichtmikroskop ist 400 Jahre alt – und seine Grenzen sind noch immer nicht ausgereizt. Zwar beschränken die Welleneigenschaften des Lichts seine Leistungsfähigkeit. Doch gelingt es Wissenschaftlern immer wieder, die Grenzen des Machbaren zu überwinden. Stefan Hell, Direktor am Max-Planck-Institut für biophysikalische Chemie in Göttingen, hat ein neues Kapitel der Lichtmikroskopie geschrieben.
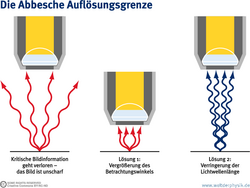
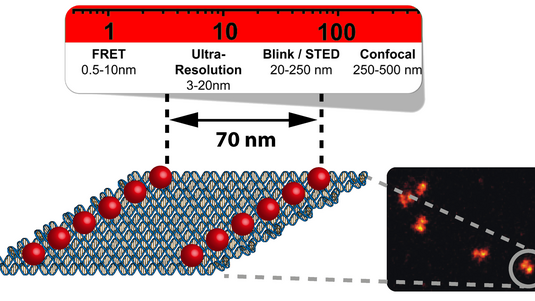
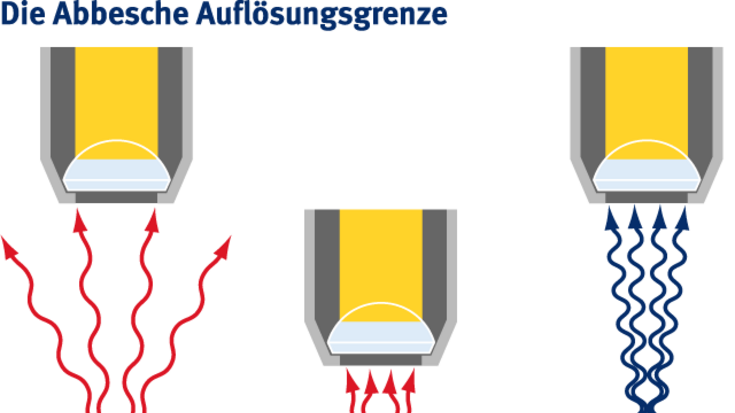
Eigentlich war es eine Tatsache, an der es nichts zu rütteln gab. Ernst Abbe erkannte 1873, dass Objekte, die enger als 200 Nanometer (Milliardstel Meter) beieinander liegen, nicht voneinander getrennt abgebildet werden können. Denn Objekte unterhalb der Abbeschen Beugungsgrenze – der Hälfte der Wellenlänge des Lichts – würden im Bild immer als ein einziger verwaschener Fleck erscheinen. Die Auflösung optischer Mikroskope ist durch die Welleneigenschaften des Lichts also generell begrenzt.
Elektronen- und Rasterkraftmikroskope erreichen zwar die gewünschte Auflösung. Aber Elektronenmikroskope arbeiten unter Vakuum und teilweise bei tiefen Temperaturen – eine Tortur, bei der keine untersuchte Zelle am Leben bleibt. Rasterkraftmikroskope hingegen funktionieren unter lebensfreundlicheren Bedingungen. Dafür können sie nur die Oberfläche eines Objektes abtasten.
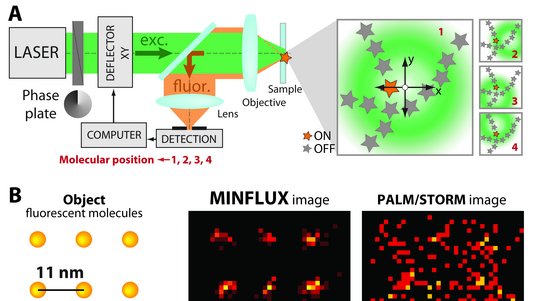
Die wichtigste bildgebende Methode in der biomedizinischen Grundlagenforschung ist die Fluoreszenzmikroskopie, eine spezielle Form der Lichtmikroskopie. Hierbei wird eine mit Fluoreszenzmolekülen markierte Probe mit Laserlicht einer bestimmten Wellenlänge bestrahlt. Die Moleküle absorbieren das Licht und geraten vom Grundzustand in einen angeregten Energiezustand. Kurz darauf fallen sie spontan in den Grundzustand zurück und senden dabei Licht aus – das „Fluoreszenzlicht“. Es ist etwas energieärmer, also langwelliger, als das Anregungslicht.
Unterschiedliche Strukturen einer Probe lassen sich zum Beispiel mit verschiedenen Farbstoffen markieren und dank ihrer charakteristischen Fluoreszenz abgesetzt vom Rest untersuchen. Wollten Wissenschaftler jedoch biologische Vorgänge auf der Nanoskala beobachten, stand ihnen wie auch bei anderen Lichtmikroskopen die Abbesche Beugungsgrenze im Weg. Die Objekte der wissenschaftlichen Begierde sind einfach kleiner als die Wellenlänge des Lichts und daher mit klassischen Abbildungsmethoden nicht zugänglich.
Grenzen überwinden
Stefan Hell jedoch wollte sich nicht damit zufrieden geben. Der Physiker am Max-Planck-Institut für biophysikalische Chemie in Göttingen stieß während seiner Promotion Ende der 1980er Jahre auf das Problem der Auflösungsbegrenzung und arbeitet seitdem leidenschaftlich an dessen Überwindung. Könnte man die Beugungsgrenze nicht doch durchbrechen und die Lichtmikroskopie auf der Nanoskala anwenden? Hell brachte erste Gedanken zu Papier, entwarf physikalische Konzepte und ließ seine Überlegungen schließlich patentrechtlich schützen. „Es war Intuition“, sagt der Wissenschaftler heute. „Ein sicheres Gefühl, dass das letzte Wort noch nicht gesprochen und vor allem die Fluoreszenzmikroskopie noch nicht ausgereizt war.“
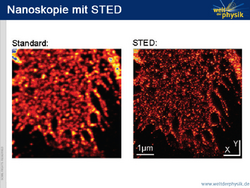
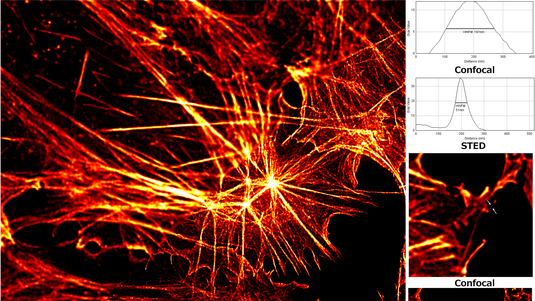
Sein Gefühl hat ihn nicht getäuscht: Aus seinen ersten Gedanken entwickelte Stefan Hell die 4Pi-Mikroskopie, mit der er die Auflösung entlang der Ausbreitungsrichtung des Lichts um das Siebenfache verbesserte. Drei Jahre darauf formulierte er das Konzept der STED-Mikroskopie (engl. STimulated Emission Depletion, „stimulierte Emissions-Löschung“): das erste physikalisch schlüssige Konzept zur Überwindung der Abbeschen Grenze. Heute lassen sich beide Methoden kombinieren. So gelang es Hells Team aus Physikern, Chemikern, Biologen und Ingenieuren, mit hoch aufgelösten 3-D-Bildern aus einem STED-4Pi-Fluoreszenzmikroskop tatsächlich das Tor zur Nanowelt für die Lichtmikroskopie aufzustoßen. Dabei eröffnet STED der Forschung so vielfältige Möglichkeiten, dass das Wissenschaftsmagazin Nature Methods STED zur Methode des Jahres 2008 kürte.
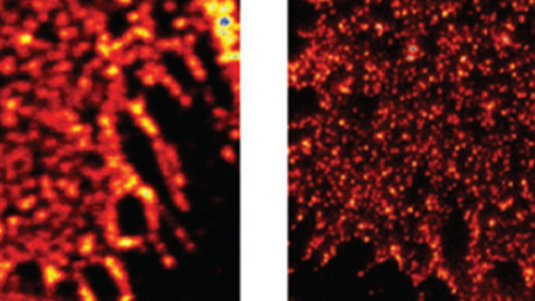
Der entscheidende Schritt der STED-Mikroskopie beruht nicht auf Licht, sondern auf Dunkelheit. Denn das Abbesche Gesetz der Abbildungsgrenze hat nach wie vor Gültigkeit: Bringt man die gesamte Probenoberfläche zum Leuchten und betrachtet sie unter dem Mikroskop, sieht man keine Strukturen kleiner als 200 Nanometer – egal wie findig das Linsensystem konstruiert sein mag. Mit einem Trick lässt sich die Abbildungsgrenze allerdings umgehen. Dieser besteht darin, die angeregten Leuchtmoleküle in einem ringförmigen Bereich gezielt so abzuschalten, dass nur noch ein winziger Fleck der Probe fluoresziert. Mit dem richtigen Abschaltmechanismus kann dieser helle Fleck durchaus kleiner sein als die von Abbe gefundene untere Grenze.
STED - das Licht im Dunkel
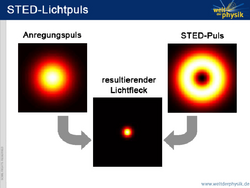
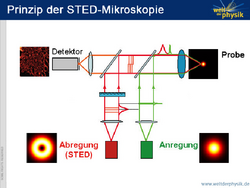
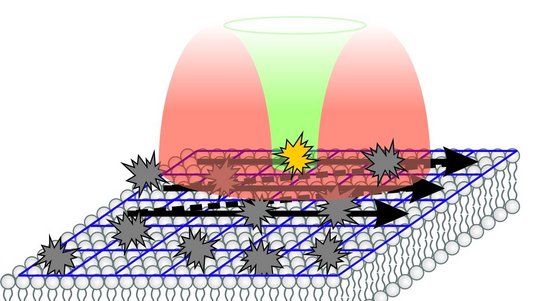
Wie bei der herkömmlichen Fluoreszenzmikroskopie werden die Moleküle der Probe zunächst in einer möglichst kleinen Region mit einem Lichtpuls angeregt. Dieser erste Lichtpuls ist natürlich auch der Abbildungsgrenze unterworfen und kann deswegen nicht beliebig verkleinert werden. Zur gezielten Abschaltung der Fluoreszenzmoleküle wird dann direkt nach dem ersten Lichtpuls ein zweiter Puls geschickt, der sogenannte STED-Puls. Trifft ein Photon des STED-Pulses auf ein angeregtes Molekül, wird dieses gezwungen, selbst ein Photon abzugeben. Dieser Vorgang heißt „stimulierte Emission“. Danach ist das Molekül nicht mehr angeregt und kann somit auch nicht fluoreszieren – es ist gewissermaßen „abgeschaltet“. Der zweite, abregende Lichtstrahl ist in der Mitte viel schwächer als an seinem Rand. Daher schaltet er die Fluoreszenzmoleküle in einem ringförmigen Gebiet ab, in dessen Zentrum eine leuchtende Kreisfläche übrig bleibt.
Die Größe der leuchtenden Fläche hängt in diesem Fall nicht mehr von der Beugungsgrenze ab, sondern allein von der Intensität des abregenden STED-Pulses. „Je intensiver der STED-Puls ist, desto besser regt er ab“, sagt Hell. „Überschreitet die Intensität eine gewisse Schwelle, hat das Molekül kaum eine Chance, spontan zu fluoreszieren. Man sagt, die Abregung ist gesättigt. Wird die Intensität weiter gesteigert, nimmt der von der Abregung betroffene Bereich immer weiter zu – die fluoreszierende Region wird immer weiter eingeschnürt.“
Für Hell ist das der eigentliche Trick des Verfahrens: „Je mehr man die Sättigungsschwelle überschreitet, desto kleiner wird der Fluoreszenzfleck und umso besser kann man auflösen.“ Überschreitet man die Abschaltschwelle der Fluoreszenzmoleküle beispielsweise um das Neunfache, so verdreifacht sich die Auflösung in etwa. Überschreitet man sie um das Hundertfache, ist der Auflösungsgewinn rund verzehnfacht. Man braucht dazu jedoch Fluoreszenzmoleküle, die eine möglichst niedrige Abregungsschwelle haben. Denn eine zu hohe Intensität des STED-Pulses würde die Moleküle zerstören.
Jeder Punkt auf der Probe lässt sich dank der neuen Methode mit einer Auflösung deutlich unter derjenigen konventioneller Lichtmikroskope abbilden. Winzige leuchtende Bereiche, die kleiner als die Abbildungsgrenze sind, bleiben in einem Meer aus Dunkelheit übrig. Ist ein Fleck untersucht, nimmt man sich einfach den nächsten vor. Aus den einzeln aufgenommenen Lichtflecken kann ein Computer dann ein Bild der gesamten untersuchten Probe zusammensetzen.
„Die Beugung des Lichts verschwindet natürlich nicht, aber sie ist nicht mehr die Grenze“, sagt der Erfinder der neuen Technik. Ohne physikalische Gesetze zu verletzen, könne man nun einen Fluoreszenzfleck von der Größenordnung eines Moleküls erzeugen und damit Auflösungen bis hinunter zur molekularen Skala erreichen.
Ein Konzept – viele Möglichkeiten
Die bereits erfolgreiche STED-Mikroskopie ist eine Variante eines viel allgemeineren Konzepts, genannt RESOLFT. Die Abkürzung kommt aus dem Englischen (reversible saturable/switchable optical (fluorescent) transitions) und beschreibt das systematische Ausschalten von Fluoreszenzmolekülen, um die Beugungsgrenze auszuhebeln. Und so arbeitet das Team um Stefan Hell bereits an Alternativen zu STED. Statt die Randmoleküle gezielt aus dem angeregten Energiezustand abzuregen, ist es beispielsweise möglich, sie schon vor der eigentlichen Fluoreszenzanregung aus dem Grundzustand zu entfernen. In Betracht ziehen die Forscher außerdem, in den Molekülen bestimmte Atomgruppen, welche die Fluoreszenz ein- und ausschalten, mithilfe von Licht umzulagern.
 Film aus STED-Aufnahmen
Film aus STED-Aufnahmen
Film: Leben auf der Nanometer-Skala
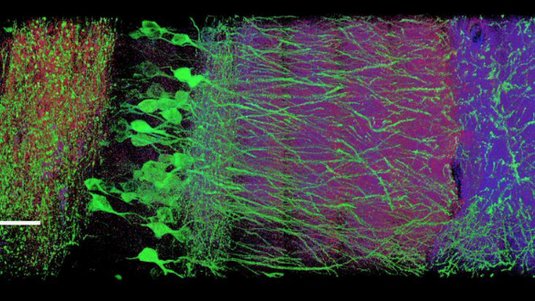
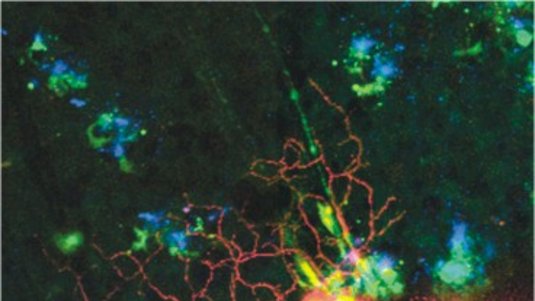
Erstellt man die Aufnahmen an einem STED-Mikroskop schnell genug, lassen sich die einzelnen Bilder sogar zu einem Film zusammensetzen. Auf diese Weise konnten die Forscher des MPI dem Leben auf der Nanometerskala inzwischen live bei der Arbeit zusehen: Im Jahr 2008 filmten sie den Transport von Botenstoffen in lebenden Nervenzellen und ließen so den Traum vieler Biologen Wirklichkeit werden.
Die Lichtmikroskopie stellt für die Biowissenschaften die einzige Möglichkeit dar, das Innere lebender Zellen und die darin ablaufenden Prozesse zu beobachten. Dank der neuen Abbildungskonzepte sind den Forschern nun völlig neue Einblicke in die Welt des Lebens auf der Nanoskala möglich. „Am Anfang“ erinnert sich Stefan Hell, „wollte kaum jemand daran glauben. Aber jetzt ist klar: Die Vision der lichtoptischen Nanoskopie ist Wirklichkeit geworden.“
Die 4pi-Mikroskopie
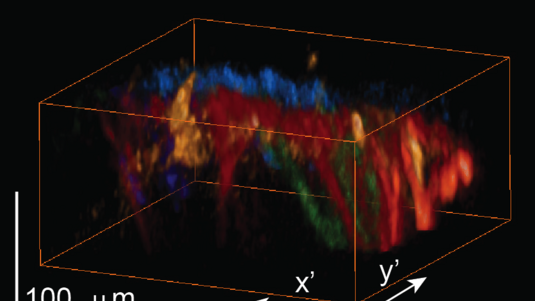
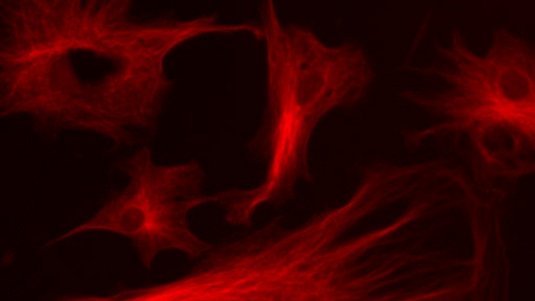
Schon mit dieser Methode gelang es, die optische Auflösung von den vorher möglichen 500 Nanometern auf 70 bis 140 Nanometer entlang der optischen Achse zu verbessern. Zwar blieb die Abbesche Beugungsgrenze noch unangetastet, doch mit der 4Pi-Idee hatte Stefan Hell Anfang der 1990er Jahre erstmals gezeigt, dass die Lichtmikroskopie noch lange nicht am Ende ist. Obwohl er die Theorie der Methode schlüssig bewiesen hatte, glaubte zunächst allerdings kaum jemand, dass sie in der Praxis umsetzbar sei. Die Göttinger Max-Planck-Forscher bewiesen das Gegenteil und gewannen mit der 4Pi-Mikroskopie beispielsweise hochaufgelöste 3-D-Bilder von Proteinen im sogenannten Golgi-Apparat - das sind Zellorganellen, in denen Proteine sortiert und verzuckert werden (siehe Foto).
Statt eines einzigen Objektivs, so der Grundgedanke der 4Pi-Mikroskopie, verwendet man zwei Objektive, die gegeneinander gerichtet sind. Die Lichtwellen beider Objektive werden so überlagert, dass sie im Fokuspunkt ihr Feld verstärken (konstruktive Interferenz). Auf diese Weise simuliert man eine beinahe kugelförmige Lichtwelle, die fast aus allen Richtungen auf den Fokuspunkt zuläuft. Der volle Raumwinkel von 4Pi wird dadurch viel besser abgedeckt.
Die Wissenschaftler um Hell sind überzeugt, dass es sich lohnt, das Auflösungsproblem systematisch und von mehreren Seiten anzugehen. Unabhängige Ansätze wie die STED- und die 4Pi-Mikroskopie könnten dann kombiniert werden und würden sich gegenseitig ergänzen.
Quelle: https://www.weltderphysik.de/gebiet/materie/analyse-von-materialien/optische-mikroskopie/lichtblicke-in-die-nanowelt/