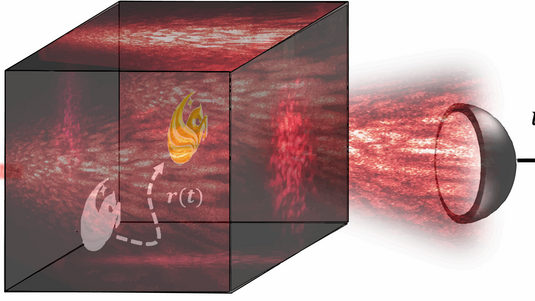
Zusammenstöße von Atomen bei Diffusion verfolgt

Vor fast 200 Jahren beobachtete der schottische Arzt und Forscher Robert Brown die Zitterbewegung von Pollen in einer Flüssigkeit. Ähnlich wie der Blütenstaub verteilen sich auch Moleküle oder Atome in Gasen und Flüssigkeiten: Die einzelnen Teilchen stoßen zusammen, breiten sich dadurch aus und durchmischen sich. Dieser Prozess wird als Diffusion bezeichnet. Physiker haben nun die fundamentalen Schritte bei der Diffusion einzelner Atome in einem Gas beobachtet und theoretisch beschrieben, wie sie in der Fachzeitschrift „Physical Review Letters“ berichten.
Für ihr Experiment verwendeten Michael Hohmann von der Technischen Universität Kaiserslautern und seine Kollegen einzelne Cäsiumatome, die fast am absoluten Temperaturnullpunkt in ein Gas aus einigen Tausend Rubidiumatomen diffundierten. „Wir haben ein sehr kaltes, dünnes Gas verwendet, um die Frequenz der Stöße drastisch herunterzusetzen“, erläutert Hohmann. Zu verschiedenen Zeiten bestimmten die Forscher die Position der Cäsiumatome im umgebenden Gas und konnten so darauf schließen, wie sich die Bewegungen der Atome durch Kollisionen mit den Rubidiumatomen veränderten. Diese extrem verlangsamte Diffusion wollten die Forscher auch theoretisch beschreiben. Doch vereinfachte Modelle der Diffusion vernachlässigen die einzelnen Zusammenstöße von Teilchen. „In diesem Zusammenhang sprechen wir auch von einem kontinuierlichen Medium, in das etwa ein größeres Teilchen hineindiffundiert. Diese Vereinfachung ist umso besser, je kleiner die Masse der Teilchen im Medium und je größer die Frequenz der Zusammenstöße ist“, so Hohmann.
Im nun durchgeführten Experiment kam es aber nur selten zu Kollisionen. Zudem besitzen Rubidium- und Cäsiumatome fast die gleiche Masse. Zur Überraschung der Forscher ließ sich das vereinfachte kontinuierliche Modell aber dennoch anwenden – mit einer einzigen Modifikation: Die effektive Viskosität des Mediums hängt von der Geschwindigkeit des diffundierenden Atoms ab. Mit diesem abgewandelten Modell ließen sich auch reale Situationen beschreiben, wie etwa die Diffusion von Aerosolen – winzigen Schwebeteilchen – in den dünnen Luftschichten der oberen Atmosphäre oder von Gas im interstellaren Raum.
Pressemitteilung der Technischen Universität Kaiserslautern
Quelle: https://www.weltderphysik.de/gebiet/materie/nachrichten/2017/einzelne-zusammenstoesse-von-atomen-bei-diffusion-verfolgt/