Wie Diamant weich wird
Wissenschafter können erstmals erklären, warum sich das härteste Material der Welt schleifen lässt
Freiburg - Diamant ist das härteste Material, dass wir kennen und dient heute als ein unverzichtbares Industrie-Werkzeug. Trotzdem lässt auch er sich schleifen. Forscher am Fraunhofer-Institut für Werkstofftechnik konnten nun erstmals erklären, warum sich die Edelsteine trotz ihrer Härte überhaupt bearbeiten lassen.
Diamanten bestehen ausschließlich aus Kohlenstoffatomen und verdanken ihre Festigkeit einer speziellen Kristallstruktur: Jedes Kohlenstoffatom bildet Bindungen mit je vier anderen Kohlenstoffatomen aus. Diese Bindungen sind alle gleich stark und ragen tetraedisch in den Raum. Bindungen und Atome haben so den maximal möglichen Abstand zueinander. Ihre Abstoßung ist deshalb gering und die Bindungen sind folglich sehr stabil.
Diamanten werden industriell mit Hilfe anderer Diamantsplitter bearbeitet. Dies funktioniert allerdings nur, wenn der zu schleifende Diamant sich in einem bestimmten Winkel zum Schleifrad befindet. Handwerker sprechen in diesem Zusammenhang häufig von weichen und harten Diamantseiten, Naturwissenschaftler bezeichnen das Phänomen als Anisotropie.
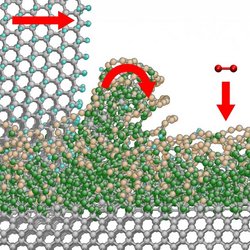
Die Forschergruppe um Lars Pastewka und Stefan Moser vom Fraunhofer Institut für Werkstoffmechanik konnte nun enträtseln, wie diese Anisotropie der Diamanten erklärt werden kann, indem sie ein mathematisches Modell entwickelten, welches die Kraftfelder zwischen den einzelnen Atomen modelliert. Auf Basis dieses Modells haben sie die Bahnen von rund 10.000 Kohlenstoffatomen an der Grenzfläche der Diamanten berechnet. Mit ihren Ergebnissen lassen sich sämtliche Phänomene erklären, die beim Schleifen von Diamanten auftreten: Durch die Reibung zwischen Diamantsplittern und dem Rohdiamanten bildet sich eine neue, glasartige Kohlenstoffphase auf der Oberfläche des Diamanten. Diese ist in dem Moment gewissermaßen kein Diamant mehr. Die entstehende Kohlenstoffphase ist weniger fest gebunden und die Spitzen der Diamantsplitter können sie abkratzen. Wie schnell besagte Phase entsteht, hängt entscheidend von der Orientierung des Rohdiamanten ab und erklärt also die Anisotropie.
Aber noch einer zweiter Effekt trägt dazu bei, dass die oberste Schicht des Edelsteins sich abtragen lässt: Den Kohlenstoffatomen der Oberfläche fehlt häufig der vierte Bindungspartner. Deshalb sind sie weniger stark gebunden und in der Lage weitere Bindungen einzugehen zum Beispiel mit Sauerstoffatomen aus der Luft. Die O2-Moleküle verbinden sich mit den Kohlenstoffatomen zu Kohlenstoffdioxid und lösen sie so vom Kristallgitter.
Welt der Physik
Quelle: https://www.weltderphysik.de/gebiet/materie/nachrichten/2010/wie-diamant-weich-wird/