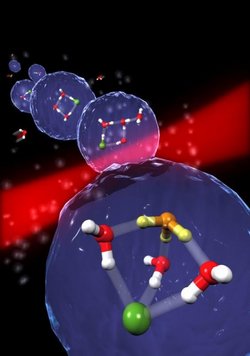
Ätzendes Wasser: Forscher erschaffen weltkleinsten Tropfen Salzsäure
Nur vier Wassermoleküle sind nötig, um aus Chlorwasserstoff einen winzigen Salzsäuretropfen zu bilden
Bochum - Als Aqua caustica – ätzendes Wasser – ist Salzsäure bereits seit über 400 Jahren bekannt. Nun fanden deutsche Wissenschaftler heraus, dass mindestens vier Wassermoleküle nötig sind, um aus Chlorwasserstoff (HCl) tatsächlich Salzsäure zu erhalten. Wie sie in der Zeitschrift "Science" berichten, schufen sie dabei den kleinsten Salzsäuretropfen der Welt. Dieser Prozess der Säurebildung hat große Bedeutung für das Verständnis chemischer Prozesse auf der Nanoskala.
"Während wir alle Säuren aus dem Alltag kennen, haben wir jetzt erstmals auf molekularer Ebene Säurebildung direkt beobachtet", sagt Martina Havenith-Newen von der Ruhruniversität in Bochum. Dazu kühlten sie ein HCl-Moleküle fast bis auf den absoluten Nullpunkt bei minus 273 Grad Celsius ab. Ohne Wasser wird HCl allerdings nicht zur Säure. Daher fügten sie einzelne Wassermoleküle hinzu. Exakt beim vierten Molekül gab HCl ein Proton an ein Wassermolekül ab und es bildete sich das so genannte Hydroniumion H3O+. Erst dieses Ion macht eine Säure aus. Seine Konzentration wird mit dem pH-Wert angegeben.
Um diesen Prozess der Säurebildung auf atomarer Skala zu beobachten, nutzen die Forscher Infrarotlaser. Es zeigte sich, dass Chlorwasserstoff trotz der extrem kalten Umgebung ein Proton an ein Wassermolekül abgeben konnte. Simulationsrechnungen bestätigten, dass genau vier Wassermoleküle um ein einzelnes Chlorwasserstoffmolekül nötig sind, um ein einziges Proton umzulagern. "Dieses Wissen brauchen wir auch, um chemische Prozesse in nanoskopischen Strukturen, auf kleinen Partikeln oder auf Oberflächen verstehen zu können", erklärt Havenith-Newen. Zudem gebe es eine reichhaltige Chemie bei sehr tiefen Temperaturen - eine zentrale Grundlage für Reaktionen auf stratosphärischen Wolken oder im Weltraum. Mit diesem Ergebnis können Chemiker in neue Bereich vorstoßen. Denn bisher wussten sie nicht, wie Reaktionen mit ganz wenigen Wassermolekülen bei ultrakalten Temperaturen überhaupt stattfinden konnten.
Wissenschaft aktuell
Quelle: https://www.weltderphysik.de/gebiet/materie/nachrichten/2009/aetzendes-wasser-forscher-erschaffen-weltkleinsten-tropfen-salzsaeure/