Wie der Muskel im Innersten zuckt
Neue Interferometrie-Technik zeigt Kontraktion erstmals auf Molekularebene
Florenz (Italien)/Grenoble (Frankreich) - Elektrische Spannung lässt ein Froschbein wie lebendig zucken. Dieses Jahrhunderte alte Schulbuchbeispiel konnte ein internationales Forscherteam nun erstmals tief im Muskelinneren betrachten. Eine neue Röntgeninterferometrie-Technik macht auf der Molekül-Ebene sichtbar, wie die Muskeleiweiße ihre Form und Struktur verändern, wenn sich eine einzelne, intakte Muskelzelle zusammenzieht. Sie präsentieren die Details in den "Proceedings of the National Academy of Sciences". Die Erkenntnisse könnten verstehen helfen, wie Muskelzellen auf unterster Ebene kommunizieren und wie die Signalmechanismen bei Herzanfällen versagen.
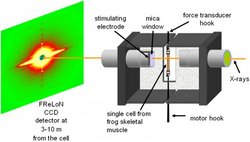
"Da wir Muskeln für Bewegung, Atmen und Körperhaltung brauchen, ebenso wie für den Schlag des Herzens, ist das Verstehen dieser Mechanismen von großer Bedeutung in der Biologie und Medizin", erklärt Malcolm Irving vom Londoner King's College. Gemeinsam mit Kollegen der italienischen Università di Firenze und der European Synchrotron Radiation Facility (ESRF) in Grenoble hatte er die extrem schnell ablaufenden Prozesse sichtbar machen können. Das Team nutzte dazu die so genannte Röntgeninterferometrie, eine neue Technik, bei der Röntgenstrahlen unter einem sehr flachen Winkel auftreffen, gestreut werden und später durch Überlagerung Details sichtbar machen. Nötig sind dafür besonders intensive und eng gebündelte Röntgenstrahlen, wie sie das ESRF-Synchrotron liefert.
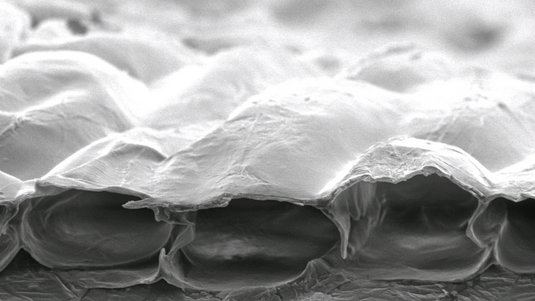
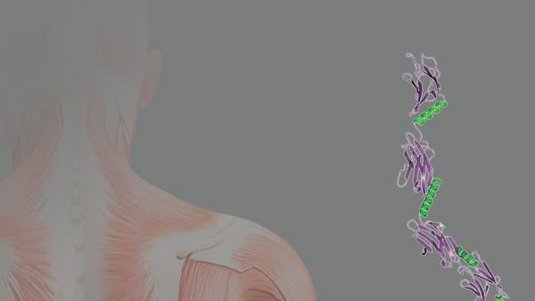
"Wir beobachteten ziemlich schnelle biologische Prozesse, im Bereich von Millisekunden, mit minimalen Strukturveränderungen von typischerweise zehn Nanometern oder weniger. Ein menschliches Haar ist zehntausend Mal dicker", ergänzt Ko-Autor Vincenzo Lombardi von der Università di Firenze. In einer Muskelzelle sitzen zwei Arten von Fasern oder Filamenten: Die einen bestehen aus dem Eiweiß Aktin, die anderen aus dem Eiweiß Myosin. Wenn sich diese Filamente gegeneinander verschieben, das außenliegende dickere Aktinfilament gegen das innenliegende dünnere Myosinfilament, so zieht sich der Muskel zusammen. Dazu schickt das Hirn ein Nervensignal an die Muskelzelle. Diese startet daraufhin eine Kette interner Abläufe, die in Veränderungen der chemischen Struktur - und damit der Form - der Actin- und Myosin-Fasern endet.
Was dabei genau mit den Muskeleiweiß-Molekülen geschieht, konnten die Forscher in Echtzeit beobachten und damit die bisherigen Theorien bestätigen: Die kopfförmigen Enden der Myosin-Moleküle winkeln sich ab, so dass die Aktinfilamente an ihnen vorbeigezogen werden. Es zeigte sich auch, dass die Bewegungen dieser "Myosin-Motoren" deutlich langsamer ablaufen als die Strukturveränderungen der Aktinfasern. Das unterschiedliche Timing wiederum verrät den Signalpfad im Muskel zwischen beiden Fasertypen - und lässt auf den Mechanismus der Muskelregulation schließen. Einen direkten klinischen Nutzen hat dies zwar nicht, doch es dürfte das Verstehen von Herzkrankheiten verbessern, bei denen diese grundlegenden Signalmechanismen im Herzmuskel gestört sind
Wissenschaft aktuell
Quelle: https://www.weltderphysik.de/gebiet/leben/nachrichten/2011/wie-der-muskel-im-innersten-zuckt/